핵심 요약: HeartFlow FFRCT는 CT 영상과 전산유체역학으로 심장 혈류를 시뮬레이션하는 AI 의료기기다. NEJM에 실린 SCOT-HEART 시험에서 심근경색 위험을 41% 줄였고, Nature Medicine에 실린 FISH&CHIPS 연구에서 NHS 9만명의 심혈관 사망률을 14% 낮췄다. FDA De Novo 승인(2014)부터 보험 수가 확보와 나스닥 IPO(2025)까지 10년의 궤적을 추적한다.
103명에서 9만 명까지
AI 의료기기(SaMD) 업계에 "정확도 95%"를 내세우는 제품은 차고 넘친다. 대개 단일 기관 후향적 연구 하나가 근거의 전부다. 다기관 무작위 대조 시험(RCT)을 거쳐 환자 예후 개선까지 증명한 제품은 손에 꼽힌다. 거기서 한 발 더 나아가 수만 명 규모의 실사용 데이터로 결과를 재확인한 제품은 더 드물다.
HeartFlow FFRCT가 그 극소수에 든다. 2014년 FDA De Novo 승인 이후 NEJM(IF 96.2)에 실린 SCOT-HEART 시험에서 심근경색 위험 41% 감소를 입증했다. 2025년에는 Nature Medicine 게재된 FISH&CHIPS 연구가 NHS(영국 국민건강서비스) 27개 병원 9만명의 실사용 데이터로 심혈관 사망률 14% 감소를 확인했다. 7년 장기 추적 레지스트리(ADVANCE-DK)까지 더하면, AI 의료기기 중 가장 두터운 근거를 가진 제품이라 해도 과언이 아니다.
"AI SaMD 임상 유효성 해부학" 시리즈 두 번째 편. 이번에는 HeartFlow FFRCT의 기술 구조부터 임상 근거 축적, 규제와 수가, 비즈니스 성과까지 순서대로 뜯어본다.
CT 영상 위에 유체역학을 얹다
HeartFlow FFRCT를 이해하려면 FFR이 무엇인지를 먼저 알아야 한다.
관상동맥은 심장에 혈액을 공급하는 혈관이다. 이 혈관이 좁아지면 심근에 피가 제대로 가지 않는다. 이 상태가 허혈(ischemia)이다. 문제는 CT에서 혈관이 50% 좁아져 보여도 실제로 혈류가 부족한지는 영상만으로 알 수 없다는 데 있다. 해부학적 협착과 기능적 허혈이 늘 일치하는 것은 아니기 때문이다.
전통적으로 이를 확인하는 방법이 FFR(Fractional Flow Reserve, 분획혈류예비량) 측정이다. 가느다란 와이어를 허벅지 동맥으로 넣어 심장까지 밀어올린 뒤, 아데노신(혈관확장제)을 주사하고 협착 전후의 압력을 직접 잰다. 이 비율이 0.80 이하면 허혈로 판정한다. 정확하지만 침습적이고, 미국 기준 $5,000~10,000이 들며, 합병증 위험도 1~2% 있다.
HeartFlow FFRCT는 이 과정 전체를 CT 영상 하나로 대체한다.
환자가 심장 CT 혈관조영(CTA)을 찍는다. 64슬라이스 이상 CT에 조영제를 투여하는, 이미 일상적으로 시행되는 검사다. 이 영상이 HeartFlow 클라우드 서버로 올라간다.
서버에서 AI가 첫 작업을 맡는다. 딥러닝 모델(U-Net 계열 CNN)이 CT 영상에서 관상동맥을 자동 추출한다. 혈관 내벽과 외벽을 구분하고 심장 박동에 의한 흔들림을 보정하여, 약 500만 개 격자점으로 구성된 3D 혈관 모형을 만든다.
여기서부터 HeartFlow의 핵심 기술이 작동한다. 전산유체역학(CFD, Computational Fluid Dynamics)이다. 항공기 날개 주변 공기 흐름을 시뮬레이션하는 것과 같은 원리를 혈관 안 혈류에 적용한다. 나비에-스토크스 방정식(Navier-Stokes equations)이라는 유체역학의 기본 방정식을 풀어서 혈관 각 지점의 압력과 유속을 계산한다.
경계 조건 설정도 빠질 수 없다. 대동맥 입구의 혈압, 심박출량, 말초 미세혈관의 저항을 환자 데이터와 생리학적 모델로 조합한다. Murray's Law(혈관 반경의 세제곱이 유량에 비례한다는 법칙)에 따라 말초 저항을 추정하고, 아데노신 주사 시와 동일한 최대 충혈 상태(hyperemia)를 가정하여 시뮬레이션을 돌린다. 실제 카테터실에서 약물을 주입해야 하는 과정을 소프트웨어가 대신하는 셈이다.
결과물은 3D 컬러맵이다. 관상동맥 각 지점에 FFRCT 값(0.00~1.00)이 색으로 표시된다. 0.80 이하 구간이 빨간색으로 나타나면 그 부위에 기능적 허혈이 있다는 뜻이다. 처리 시간은 대략 45~60분.
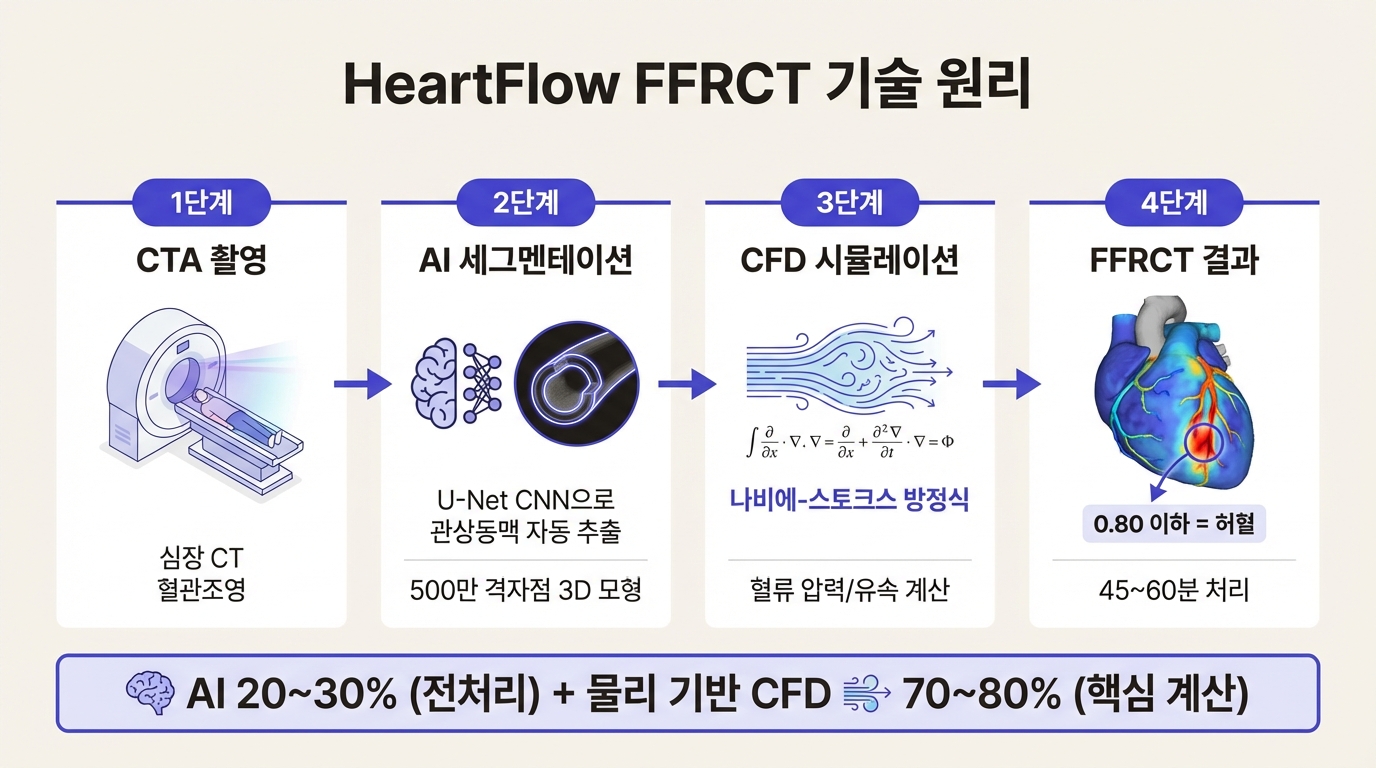
짚어둘 점이 있다. HeartFlow에서 AI의 역할은 전처리, 즉 영상 세그멘테이션과 노이즈 제거에 집중된다. 핵심 계산은 물리 기반 CFD가 담당하며, AI의 비중은 전체 파이프라인의 20~30% 정도다. 약점이 아니라 강점이다. 물리 방정식에 기반하기 때문에 설명 가능성과 재현성이 높다. FDA 승인과 임상 현장의 신뢰를 얻는 데 이 특성이 결정적으로 작용했다.
정확도에서 예후까지, 임상 근거 4단계
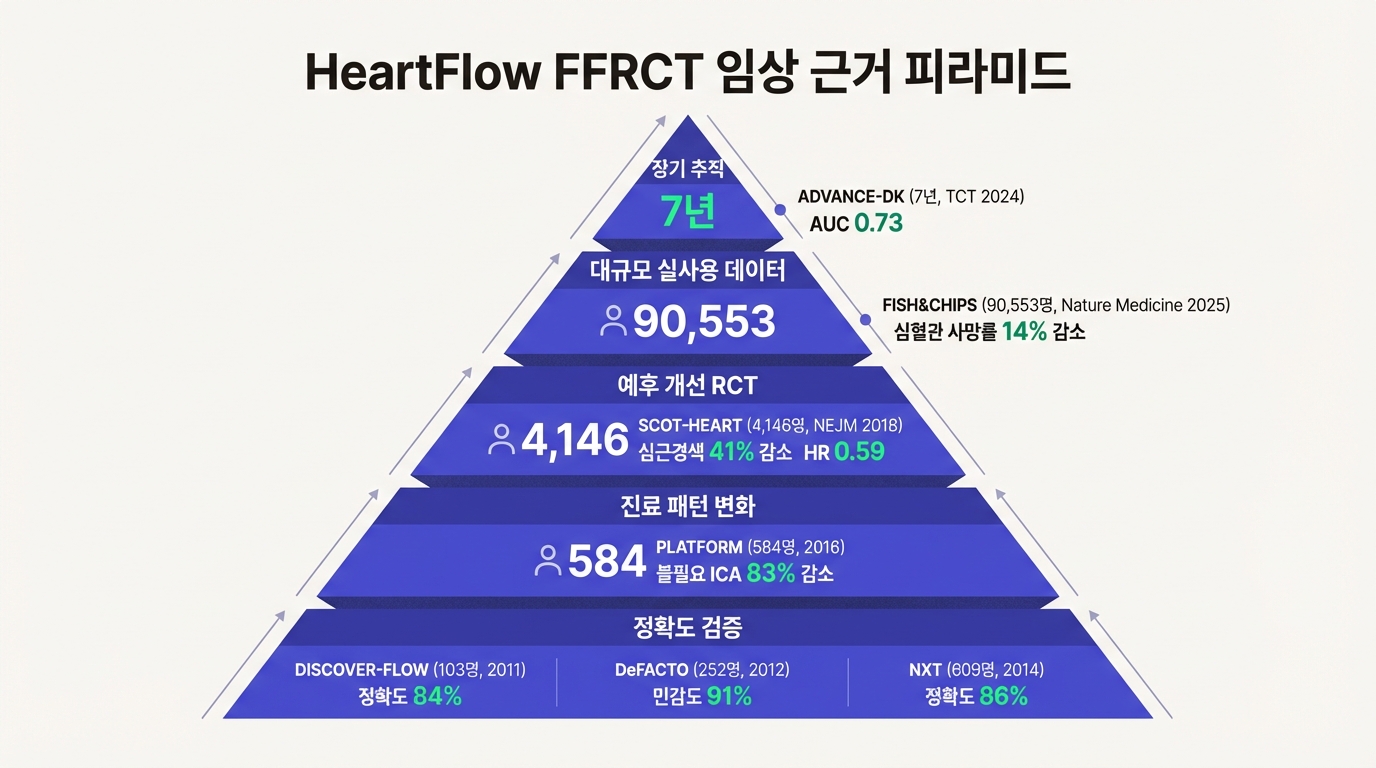
HeartFlow의 근거 축적은 교과서적인 순서를 밟았다. 정확도 검증, 진료 패턴 변화, 다기관 RCT, 대규모 실사용 데이터, 장기 추적 레지스트리.
1단계: 침습적 FFR과 얼마나 일치하는가 (2011~2014)
세 개의 연속된 시험이 FFRCT의 진단 정확도를 확인했다.
DISCOVER-FLOW(2011, 103명)가 첫 다기관 검증이었다. 환자 수준 정확도 84.3%, 민감도 87.9%, 특이도 82.2%. 비침습 방식으로도 침습적 FFR에 견줄 만한 수치가 나온다는 것을 처음 보여준 연구다.
DeFACTO(2012, 252명, 45개 기관)가 규모를 키웠다. 정확도 84%, 민감도 90.6%. 북미와 유럽 데이터를 모두 포함했다.
NXT(2014, 609명, 11개국 65개 기관)가 분수령이었다. FDA De Novo 승인의 핵심 근거가 된 3상 시험이다. 전체 정확도 86%, 민감도 87.6%, 특이도 78.2%. 관찰자 간 일치율 96%(ICC 0.94)로 재현성까지 증명했다. 누가 판독해도 거의 같은 결과가 나온다는 뜻이다.
세 시험을 관통하는 결론은 "80~90% 환자에서 FFRCT가 침습적 FFR을 대체할 수 있다"는 것이었다. 고도 석회화 환자에서는 정확도가 떨어지는 한계(약 10~20% 실패율)가 있지만, 중등도 협착 환자 대다수는 불필요한 카테터 검사를 피할 수 있다는 근거가 갖춰졌다.
2단계: 진료 현장이 실제로 바뀌는가 (PLATFORM, 2015~2016)
진단이 아무리 정확해도 임상의가 행동을 바꾸지 않으면 환자에게 돌아가는 이득은 없다. PLATFORM 시험(584명, 유럽 11개 센터)은 FFRCT가 실제 진료 패턴을 어떻게 바꾸는지 본 연구다.
결과는 명확했다. 침습적 관상동맥조영술(ICA)을 예정하고 있던 환자군에 FFRCT 가이드를 적용하자, 61%에서 침습 검사가 취소되었다. 검사를 진행한 환자 중 의미 있는 병변이 없었던 비율(불필요한 ICA)은 73%에서 12%로 떨어졌다. 83% 감소.
결정적으로, 재관류(스텐트나 우회술) 비율은 두 군에서 차이가 없었다(28.5% vs 31.6%). 시술이 필요한 환자는 빠짐없이 시술을 받았고, 필요 없는 환자만 침습 검사를 피한 것이다. "놓치는 환자가 늘어나지 않으면서 불필요한 검사만 줄었다"는 것은 진단 AI가 보여줄 수 있는 가장 이상적인 그림이다.
3단계: NEJM이 인정한 예후 개선 (SCOT-HEART, 2018)
SCOT-HEART는 규모와 추적 기간 모두에서 한 단계 올라간다. 영국 12개 병원에서 안정형 흉통 환자 4,146명을 모집하고, CTA군과 표준 치료군으로 무작위 배정하여 5년간 추적한 다기관 RCT다.
1차 종점은 관상동맥 심장질환에 의한 사망 또는 비치명적 심근경색. 5년 후 결과, CTA군 2.3%(48명) vs 표준 치료군 3.9%(81명). 위험비(HR) 0.59, 95% 신뢰구간 0.41~0.84, p=0.004. 41%의 상대위험 감소다.
흥미로운 것은 이 41% 감소의 메커니즘이다. CTA군에서 침습 검사나 재관류 시술이 더 많이 이루어진 것이 아니다. 5년 시점에서 두 군의 검사 횟수와 시술 횟수는 거의 같았다. 차이를 만든 것은 예방적 약물 치료였다. CTA로 관상동맥 상태를 정확히 파악한 의사들이 예방 약물을 더 적극적으로 처방했고(OR 1.40), 이것이 장기 예후를 바꿨다.
"더 많이 시술하는 것"이 아니라 "더 정확하게 파악하는 것"이 환자를 살린 셈이다. CTA 기반 의사결정(그리고 그 연장선에서 FFRCT 가이드)이 환자 예후를 개선한다는 최고 수준의 근거가 NEJM에 실렸다.
4단계: 9만 명의 실사용 데이터 (FISH&CHIPS, 2025)
RCT가 "통제된 환경에서 효과가 있다"를 증명한다면, 실사용(real-world) 데이터는 "일상 진료에서도 그러한가"를 확인한다. FISH&CHIPS 연구가 이 간극을 메웠다.
FISH&CHIPS는 영국 MRC(의학연구위원회) 지원으로 NHS 27개 병원에서 90,553명의 데이터를 분석한 연구다. CTA 단독 경로와 CTA+FFRCT 경로를 비교하여 2년간 추적했고, 결과는 2025년 Nature Medicine에 게재되었다.
FFRCT를 추가한 경로에서 심혈관 사망률이 14% 상대 감소했다. 전체 사망률(모든 원인)도 8% 줄었다. 불필요한 침습적 관상동맥조영술은 16%, 추가 비침습 검사는 12% 감소했다. 환자 1명당 2년간 £1,042(약 $1,394)의 비용을 절감했는데, NICE가 도입 당시 모델링한 절감 예측치를 크게 웃도는 수준이었다.
9만 명 규모의 실사용 데이터에서 사망률 감소와 비용 절감을 동시에 보여준 AI 의료기기 연구는 이 분야에서 전례를 찾기 어렵다.
7년 장기 추적이 보여주는 것 (ADVANCE-DK, 2024)
ADVANCE-DK 레지스트리는 덴마크에서 FFRCT로 평가받은 환자를 7년간 추적한 데이터다. TCT 2024 발표 결과, FFRCT 정상(허혈 없음) 환자의 7년 주요 심혈관 사건(MACE) 발생률은 5.7%였고, 허혈 환자는 16.2%였다. FFRCT와 플라크 분석을 결합하면 예측력이 더 올라갔다(AUC 0.73 vs CCTA 단독 0.63).
7년은 AI 의료기기 임상 데이터 중 가장 긴 축에 속한다. 단기 정확도가 아니라 장기 예후 예측까지 검증된 것이다.
De Novo에서 보험 수가까지, 10년의 규제 로드맵
HeartFlow의 규제 여정은 AI SaMD 기업이 참고할 수 있는 드문 선례다. 연대기순으로 살펴본다.
2011년, CE Mark 획득. 유럽에서 먼저 시장에 들어갔다. DISCOVER-FLOW 데이터가 근거였다.
2014년 11월, FDA De Novo 승인(DEN130045). 비침습적 FFR 계산이라는 카테고리가 아예 없었기 때문에, 기존 제품과의 동등성을 증명하는 510(k) 경로를 쓸 수 없었다. De Novo는 선례 없는 새로운 유형의 저-중간 위험 의료기기를 위한 경로다. NXT 시험(정확도 86%)이 핵심 근거였고, Class II로 분류되면서 이후 같은 유형 제품이 따라올 수 있는 선례가 만들어졌다.
2017년, NICE MTG32 권고(영국). NICE가 HeartFlow FFRCT를 비용효과적 기술로 권고했다. 증분비용효과비(ICER)가 영국 기준인 £20,000/QALY 미만으로 평가된 결과다. NHS가 본격적으로 도입할 수 있는 근거가 마련되었다.
2018년, CMS 수가 개시(미국). 임시 CPT 코드 0523T로 출발했다. 보험 청구가 가능해지면서 미국 내 사용량이 본격적으로 늘었다.
2024년 1월, Category I CPT 코드 75580 획득. 임시에서 정식 코드로 전환되었다. Category I은 해당 시술이 의료 현장에서 충분히 보편화되었다는 인정이다. 수가 $1,017(2025년 기준).
2024년 10월, Plaque Analysis CPT 코드 확보. FFRCT를 넘어 플라크(혈관 벽의 지방 침착물) 정량 분석에도 별도 수가를 받게 되었다. $950. UnitedHealthcare와 Cigna가 2025년 10월부터 커버리지를 시작했다.
2025년, CMS CCTA 수가 대폭 인상. CCTA(심장 CT)의 외래 수가가 $175에서 $357로 두 배 넘게 올랐다. HeartFlow에게는 직접 수가 인상이 아니지만, CCTA를 찍는 병원의 동기가 강화된다는 점에서 간접적 호재다. CCTA 촬영이 늘면 FFRCT 분석 의뢰도 자연스럽게 증가하는 구조이기 때문이다.
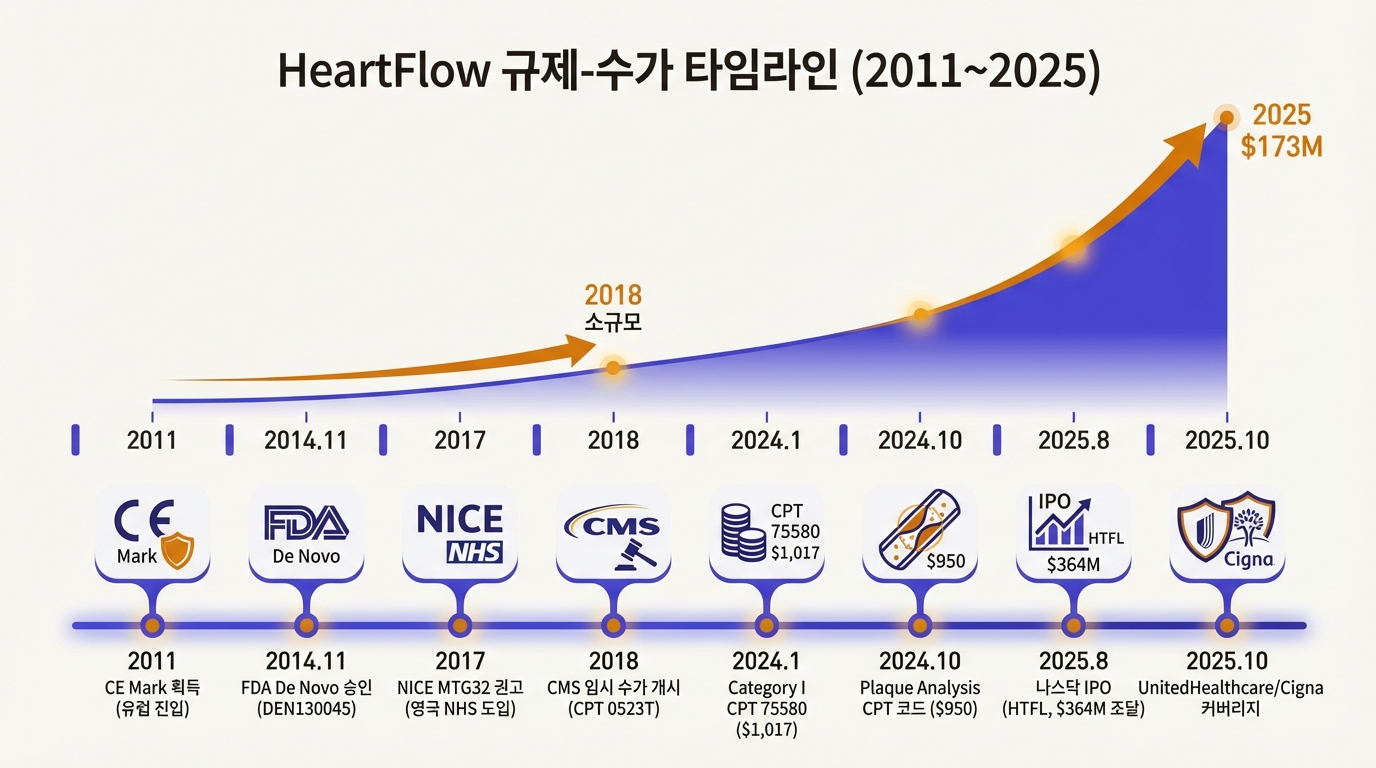
10년에 걸친 이 과정에서 패턴이 보인다. 임상 근거가 규제를 열었고, 규제가 수가를 열었으며, 수가가 시장을 열었다. NXT → De Novo → CMS 임시 수가 → SCOT-HEART → NICE 권고 → FISH&CHIPS → CPT I 코드. 각 단계가 다음 단계의 전제 조건이었다.
매출 $173M, 나스닥에 서다
보험 수가가 자리 잡자 숫자가 따라왔다.
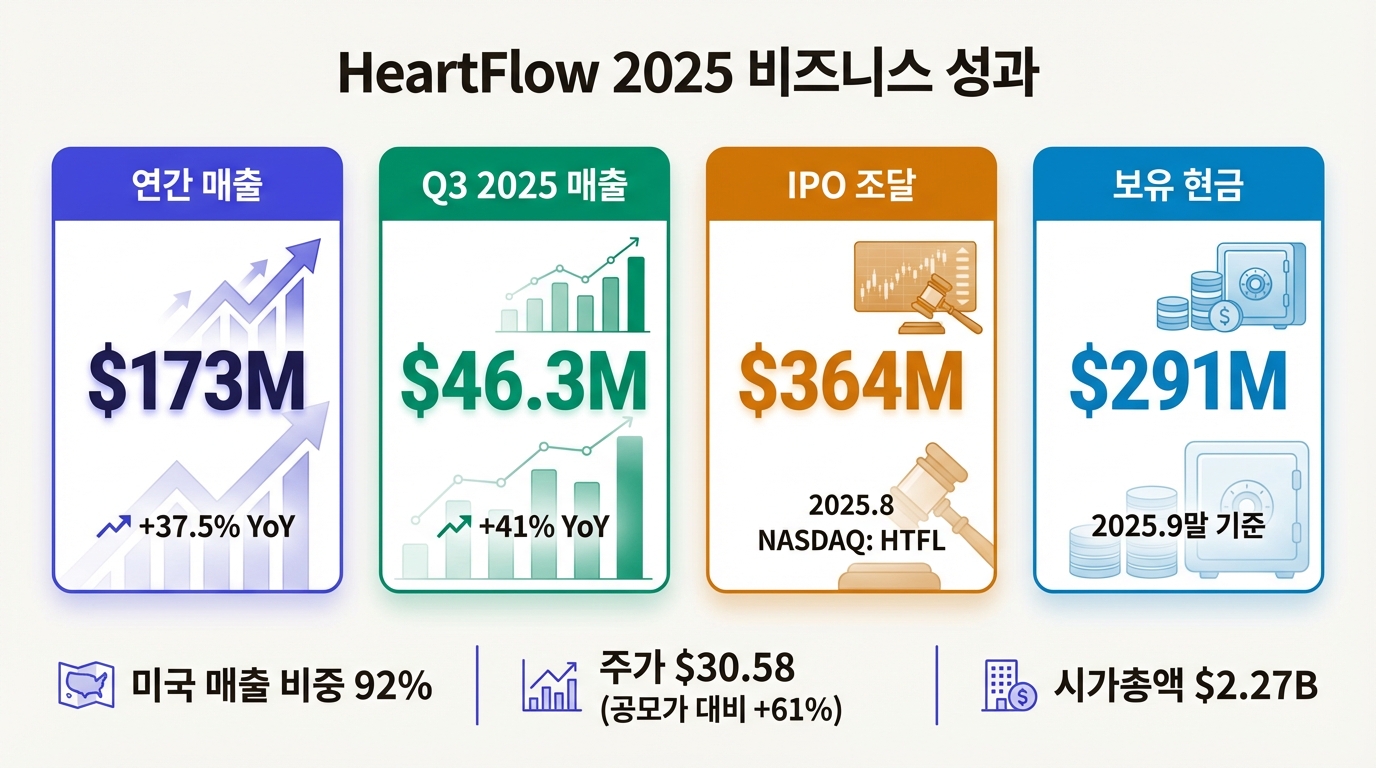
HeartFlow는 2025년 8월 7일 나스닥(NASDAQ: HTFL)에 상장했다. 공모가 $19, 당초 범위보다 $1 높았고 발행 물량도 확대했다. 총 조달 금액 $364.2M(약 4,900억원). 상장 첫날 주가가 47.4% 올라 시가총액이 $2.27B(약 3조원)에 도달했다.
2025년 3분기 매출 $46.3M, 전년 동기 대비 41% 성장. 미국 매출이 $42.5M(+42%)으로 전체의 92%를 차지한다. 연간 매출 가이던스는 $173.0~173.5M(전년 대비 +37.5~38%).
아직 흑자 기업은 아니다. Q3 영업 손실 $15.1M, Non-GAAP으로도 $11.1M 적자다. 다만 손실 폭이 전년보다 줄고 있고, IPO로 확보한 현금이 $291.2M(2025년 9월말)이어서 당분간 재무 여력은 넉넉하다. 40% 이상 매출 성장을 유지하면서 적자를 줄여가는, 고성장 의료기기 기업의 전형적 궤적이다. 2026년 2월 현재 주가는 약 $30.58로, 공모가 대비 61% 높은 수준에 있다.
매출 성장의 엔진은 두 가지다. 첫째, CCTA 사용량 자체의 증가. CMS의 수가 인상(2025)이 병원의 CCTA 촬영 동기를 강화했고, FFRCT 의뢰로 자연스럽게 이어졌다. 둘째, 플라크 분석이라는 새 수익원이다. FFRCT가 "지금 혈관이 좁은가"를 보는 기능이라면, 플라크 분석은 "앞으로 위험해질 수 있는가"를 예측하는 기능이다. UnitedHealthcare와 Cigna의 커버리지 결정(2025년 10월)으로 두 번째 성장 엔진에 불이 붙었다.
임상 근거라는 해자
HeartFlow FFRCT 사례에서 눈여겨볼 부분은, "좋은 기술"이 아니라 "좋은 근거"가 비즈니스를 만들었다는 점이다.
AI 의료기기 업계의 흔한 패턴은 이렇다. 후향적 데이터로 정확도를 입증하고, FDA 510(k)를 받고, 영업을 시작한다. 보험 수가는 나중 문제. HeartFlow는 정반대였다. 전향적 다기관 시험(DISCOVER-FLOW → DeFACTO → NXT)을 거쳐 무작위 대조 시험(SCOT-HEART)으로 예후 개선을 증명하고, 대규모 실사용 데이터(FISH&CHIPS)로 비용 절감까지 보여줬다. 이 근거가 NICE 권고, CMS 수가, 보험사 커버리지를 하나씩 열었다.
이 근거를 쌓는 데 비용이 들었다. NXT에 609명, SCOT-HEART에 4,146명, FISH&CHIPS에 90,553명. 이 규모의 임상 연구에는 수년의 시간과 수천만 달러가 필요하다. HeartFlow가 설립(2007년)에서 IPO(2025년)까지 18년이 걸린 이유 중 하나다.
수확은 지금 나타나고 있다. 근거가 두텁기 때문에 보험사가 수가를 부여했고, 수가가 있기 때문에 병원이 도입했고, 병원이 도입했기 때문에 매출 $173M과 40% 성장이 가능했다. 근거에서 규제로, 규제에서 수가로, 수가에서 시장으로 이어지는 인과 사슬이 10년에 걸쳐 완성된 것이다.
후발 주자가 이 해자를 넘으려면 같은 시간과 비용을 투입해야 한다. 기술은 빠르게 따라갈 수 있지만, NEJM과 Nature Medicine에 실린 데이터는 복제되지 않는다.
출처
- Newby DE, et al. Coronary CT Angiography and 5-Year Risk of Myocardial Infarction. N Engl J Med. 2018;379(10):924-933.
- Curzen N, et al. FISH&CHIPS: nationwide real-world evaluation of CTA+FFRCT pathway. Nature Medicine. 2025.
- Douglas PS, et al. Clinical outcomes of FFRCT-guided diagnostic strategies vs usual care (PLATFORM). Eur Heart J. 2016;37(14):1071-1081.
- Nørgaard BL, et al. Diagnostic performance of noninvasive FFRCT (NXT). J Am Coll Cardiol. 2014;63(12):1145-1155.
- Koo BK, et al. Diagnosis of ischemia-causing coronary stenoses by noninvasive FFRCT (DISCOVER-FLOW). J Am Coll Cardiol. 2011;58(19):1989-1997.
- Min JK, et al. Diagnostic accuracy of FFRCT (DeFACTO). JAMA. 2012;308(12):1237-1245.
- ADVANCE-DK Registry, 7-year outcomes. TCT 2024.
- HeartFlow Q3 2025 Financial Results. November 12, 2025.
- HeartFlow IPO Pricing. August 7, 2025.
- CMS Final Rule: CCTA OPPS reimbursement increase. November 2024.