같은 CT 영상, 다른 운명
2026년 2월, 대서양 양쪽에서 AI 의료기기 규제 문서가 동시에 나왔다. FDA는 방사선 AI 기기의 사전심사 면제를 검토하고 CDS 소프트웨어 규제를 완화했다. 같은 시기 EU는 MDCG 가이드라인으로 AI 의료기기 변경 관리 요건을 강화했다. 동일한 알고리즘이 뉴욕에서는 3개월 만에 시장에 나오고 브뤼셀에서는 18개월을 기다려야 하는 상황이 눈앞에 와 있다.
이 글에서 짚으려는 건 두 가지다. FDA의 510(k) 면제 청원과 CDS 규제 완화가 시장 진입을 어떻게 바꾸는지. EU가 왜 반대 방향을 택했고, 이 격차가 기업에게 무엇을 뜻하는지.
FDA 510(k) 면제 청원: 검증된 기업에게 열리는 패스트트랙
510(k)가 뭔가
510(k)는 FDA에 의료기기를 시판하기 전에 내는 사전 통보다. 새 제품이 이미 시판 중인 유사 제품(predicate device)과 실질적으로 동등하다는 점을 보여야 한다. FDA가 내리는 건 '허가(approval)'가 아니라 '시판 허용(clearance)'이다. PMA나 De Novo와는 다른 경로로, Class II 의료기기 대부분이 이 길을 거친다.
심사에 보통 3~6개월이 걸린다. AI/ML 의료기기는 알고리즘 검증 자료와 임상 데이터, 소프트웨어 문서가 추가로 필요해서 더 오래 걸리는 편이다. FDA가 지금까지 승인한 AI/ML 의료기기는 2025년 12월 기준 1,300건을 넘었고, 이 가운데 76%가 방사선 분야다. 2025년 한 해에만 295건이 나왔다.
청원의 골자
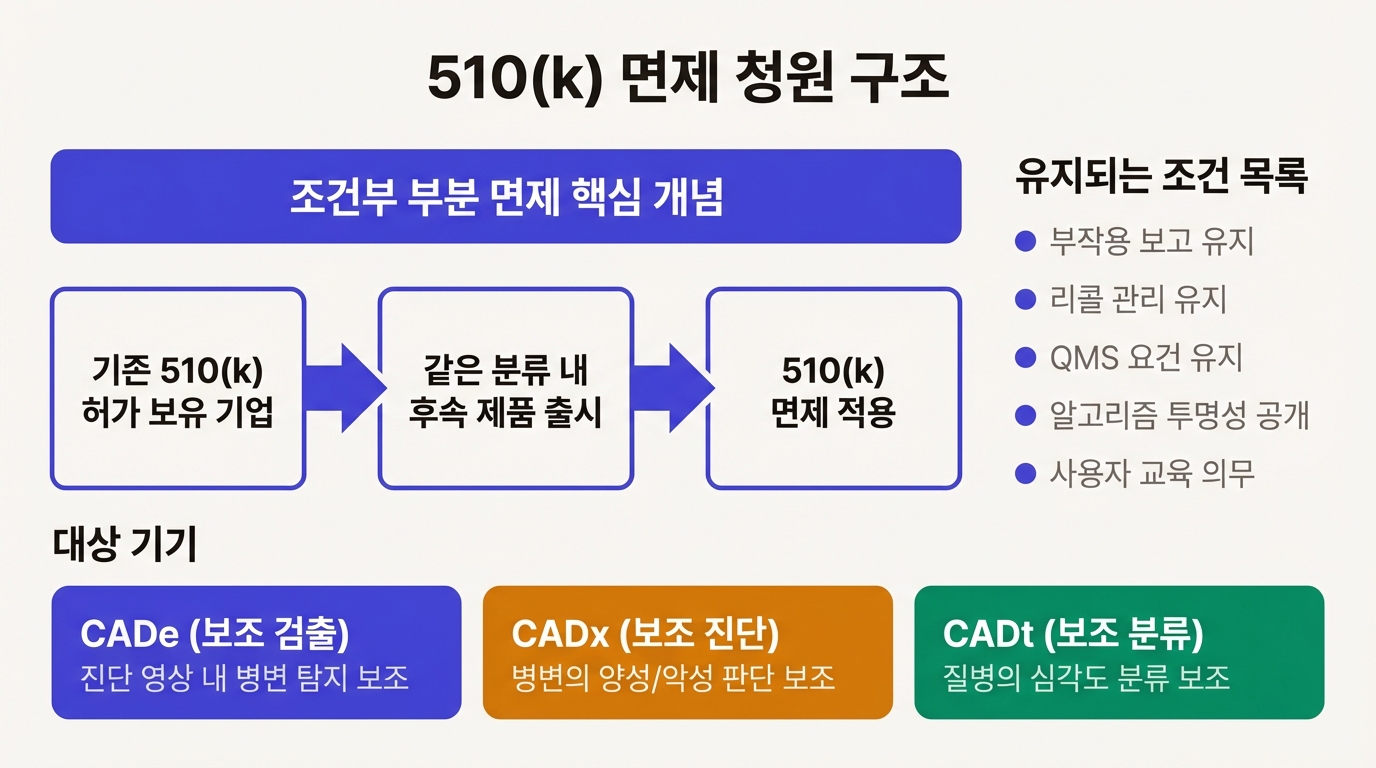
2025년 10월, 호주 AI 의료기기 기업 Harrison.ai를 대리한 Rubrum Advising이 FDA에 34페이지짜리 시민 청원을 냈다. 방사선 CADe(컴퓨터 보조 검출), CADx(보조 진단), CADt(보조 분류) 기기에 대해 510(k) 사전 통보를 부분적으로 면제해달라는 내용이다.
CADe는 폐 결절이나 유방 석회화 같은 병변을 의료 영상에서 자동으로 찾아 표시한다. CADx는 한 발 더 나아가 검출된 병변이 양성인지 악성인지 판단한다. CADt는 응급도에 따라 환자를 분류해서 어떤 케이스를 먼저 볼지 알려준다.
핵심은 '조건부 부분 면제'라는 설계다. 모든 방사선 AI 기기가 아니라, 해당 규제 분류에서 이미 510(k) 허가를 최소 1건 받은 제조사만 대상이다. 한 번 심사를 통과한 기업이 같은 분류 안에서 후속 제품을 낼 때 510(k)를 새로 제출하지 않아도 된다는 논리다.
면제가 무심사는 아니다
청원이 내건 조건은 꽤 구체적이다.
사전 심사를 줄이는 대신 시판 후 모니터링 의무를 강화한다. 부작용 보고, 리콜 관리, 품질 시스템 요건은 그대로 남는다. 알고리즘의 작동 원리, 훈련 데이터, 성능 한계를 명시적으로 공개해야 하고, 방사선 전문의 등 최종 사용자 대상 교육 프로그램도 운영해야 한다.
기존의 특별통제와 품질관리시스템(QMS) 요건도 전부 유지된다. 제품은 여전히 Class II이고, FDA 감사, 불만 처리, 부작용 보고, 등록 의무가 모두 적용된다. 사전 심사 부담을 덜어주되 사후 관리를 촘촘히 해서 균형을 잡겠다는 구조다.
청원의 행방
FDA는 2025년 12월 29일 Federal Register에 의견수렴 공고를 올렸고, 마감은 2026년 2월 27일이다. 수용 여부는 아직 모르지만, 공식 의견수렴 절차를 밟은 것 자체가 눈에 띈다. FDA가 방사선 AI 규제 효율화를 진지하게 따져보고 있다는 뜻이다.
면제가 현실이 되면 가장 먼저 혜택을 보는 건 이미 FDA 허가 이력이 있는 기업이다. Aidoc은 aiOS 플랫폼으로 다수의 510(k)를 갖고 있고, Harrison.ai는 이 청원의 당사자이며, MedCognetics는 CogNet AI-MT와 AI-MT+를 연이어 통과시켰다. 후속 제품 출시가 빨라진다.
반면 첫 제품을 준비 중인 스타트업에게는 이야기가 다르다. 기존 허가 이력이 없으면 면제 대상 자체가 되지 않는다. 이미 안에 있는 기업에게 문을 더 넓히는 구조여서, 후발주자 입장에서는 격차가 벌어지는 셈이다.
CDS 규제 완화: 답이 하나뿐인 경우

CDS란
CDS(Clinical Decision Support)는 의료진에게 진단이나 치료 관련 정보와 권고를 제공하는 소프트웨어다. 약물 상호작용 알림부터 진료 가이드라인 기반 권고, 환자 데이터 요약까지 범위가 넓다.
2016년 21st Century Cures Act는 네 가지 조건을 충족하는 CDS를 FDA 규제 대상에서 뺐다. 의료 영상이나 신호 패턴을 직접 분석하지 않을 것, 의료 전문가가 최종 결정을 내릴 것, 소프트웨어의 근거를 전문가가 독립적으로 검토할 수 있을 것, 진단이나 치료 방향을 자동 실행하지 않을 것.
2026년 1월 가이던스가 뒤집은 것
2026년 1월 6일 FDA 개정 가이던스의 가장 큰 변화는 '단일 권고' 처리 방식이다.
2022년 가이던스에서 FDA는 소프트웨어가 치료 옵션을 하나만 제시하면 의료기기로 분류했다. 여러 옵션 가운데 의료진이 고르는 구조가 아니라 결론을 하나만 내려주면 의료진의 독립적 판단을 대체한다고 봤다.
2026년 가이던스는 이 입장을 뒤집었다. 임상적으로 적절한 옵션이 하나뿐이면, 소프트웨어가 그 하나를 제시하더라도 나머지 기준을 충족하는 한 규제 재량을 행사하겠다고 밝혔다. 특정 약물 조합에서 상호작용 위험이 명백할 때 "이 약을 중단하라"고 알려주는 소프트웨어를 더 이상 의료기기로 취급하지 않겠다는 것이다.
따져보면 합리적이다. 답이 하나밖에 없는 상황에서 굳이 "여러 옵션을 보여줘야 한다"는 요건은 현실과 맞지 않았다.
영상 AI는 빠져나갈 수 없다
단서가 있다. 의료 영상(X-ray, CT, MRI)이나 신호 패턴(심전도 파형 등)을 직접 분석하는 소프트웨어는 여전히 CDS 면제 대상에서 빠진다. 영상 AI가 "이 병변은 악성 가능성이 높다"고 판단하면 CDS가 아니라 SaMD로, 510(k)나 De Novo 심사를 거쳐야 한다.
이 경계선은 얼핏 명확해 보이지만 실제로는 미묘하다. EMR 데이터를 분석해서 암 검진 권고를 내리는 소프트웨어는 CDS 면제 대상이 될 수 있다. 그런데 같은 권고라도 영상 데이터를 입력으로 쓰면 SaMD가 된다. 기능이 아니라 입력 데이터의 종류가 규제 경로를 갈라놓는다. 개발사 입장에서 설계 단계부터 신중해야 하는 이유가 여기에 있다.
EU가 반대 방향으로 간 사정
MDR과 AI Act, 이중 관문
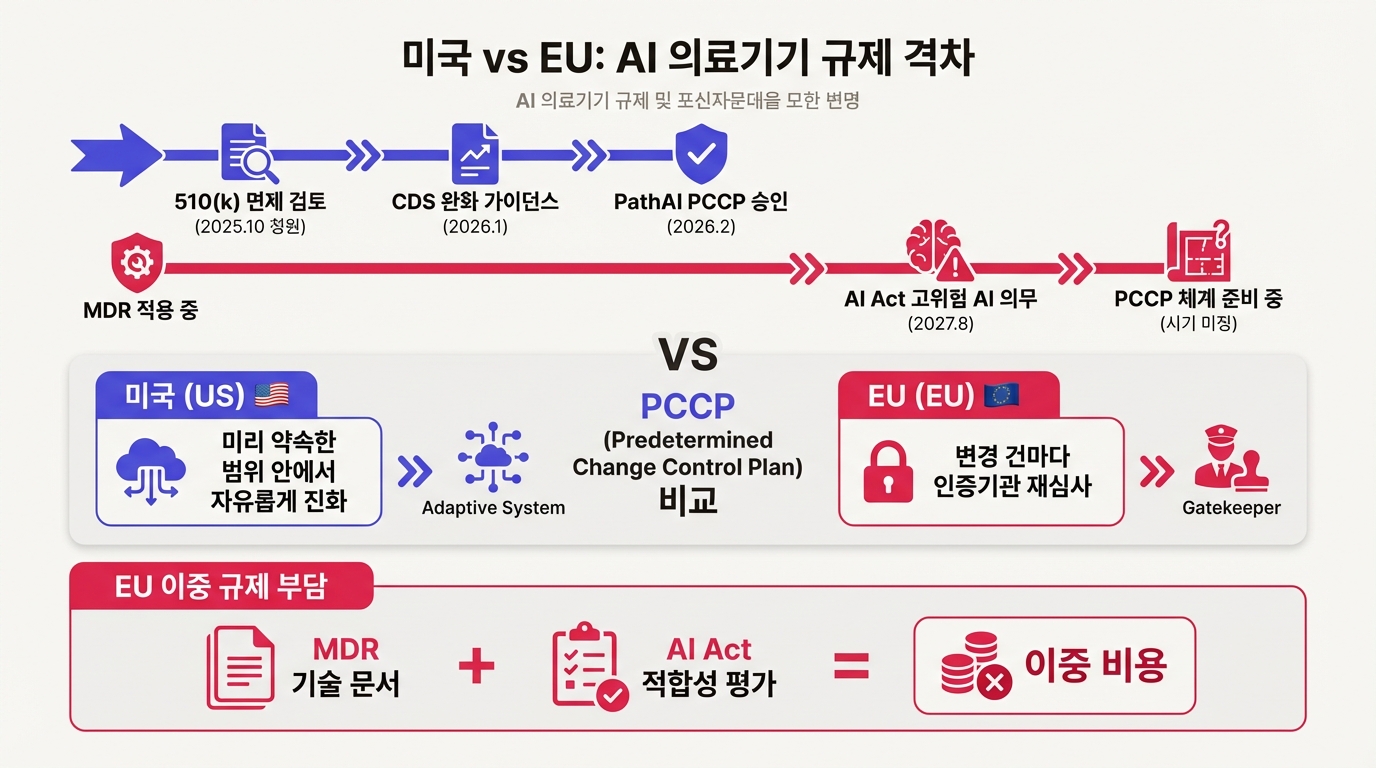
EU에서 AI 의료기기는 두 개의 규제 프레임워크를 동시에 통과해야 한다. 의료기기 규정(MDR)과 AI법(AI Act)이다.
2025년 6월 MDCG 2025-6 가이드라인이 이 두 규정의 상호작용을 구체적으로 정리했다. AI/ML 기반 SaMD는 AI Act Annex XVI에 따라 고위험 AI 시스템으로 분류된다. MDR에 따른 인증기관(Notified Body) 심사와 AI Act에 따른 적합성 평가를 모두 받아야 한다. 관문이 하나가 아니라 둘이다.
PCCP를 둘러싼 온도 차
PCCP(Predetermined Change Control Plan)는 AI 의료기기 제조사가 "앞으로 이런 범위의 변경을 이렇게 검증하겠다"는 계획을 미리 내고, 승인받으면 계획 범위 안의 업데이트를 별도 허가 없이 진행하는 체계다. AI가 데이터 축적에 따라 계속 나아져야 한다는 본질을 반영한 제도다.
미국은 이미 실행 단계에 들어섰다. PathAI Prostate가 2026년 2월 15일 510(k)를 받으면서 PCCP 승인도 함께 받았다. 전립선 생검 암 등급 분류 알고리즘을 지속적으로 업데이트할 수 있는 권한을 확보한 것이다.
EU는 다르다. PCCP에 해당하는 체계가 아직 없다. IMDRF 수준에서 가이드라인을 만들고 있고 EU가 자체 프레임워크를 준비하겠다고 했지만 시기가 불투명하다. AI Act에 따른 고위험 AI 시스템의 '중대한 변경' 의무는 2027년 8월 2일부터 본격 적용된다. 그전까지 AI 의료기기의 알고리즘 업데이트는 MDR의 기존 변경 관리 절차를 따라야 하고, 사실상 변경 건마다 인증기관 심사를 거쳐야 한다.
미국은 "미리 약속한 범위 안에서 자유롭게 진화하라"이고, EU는 "한 번 바꿀 때마다 다시 심사받아라"다.
이중 규제가 만드는 비용
EU 진출의 부담은 심사 기간만이 아니다. MDR과 AI Act를 동시에 적용하면 기술 문서를 양쪽 형식으로 따로 준비해야 한다. AI 의료기기를 심사할 수 있는 Notified Body는 TUV SUD 같은 소수 기관에 몰려 있어 병목이 심하다. EU 의료기기 데이터베이스 EUDAMED도 아직 완전히 돌아가지 않아 실시간 승인 추적조차 어렵다.
2026년 2월 12일 IMed Group과 Firefinch Software가 'Smart Code, Safe Care'라는 백서를 내놓으며 UK-US-EU 3개 시장 동시 출시 전략을 제시했다. 이런 백서가 나온다는 것 자체가 3개 시장의 규제 편차가 기업에게 상당한 부담이라는 반증이다.
규제 격차가 기업 전략에 미치는 영향
미국 먼저, 가 굳어진다
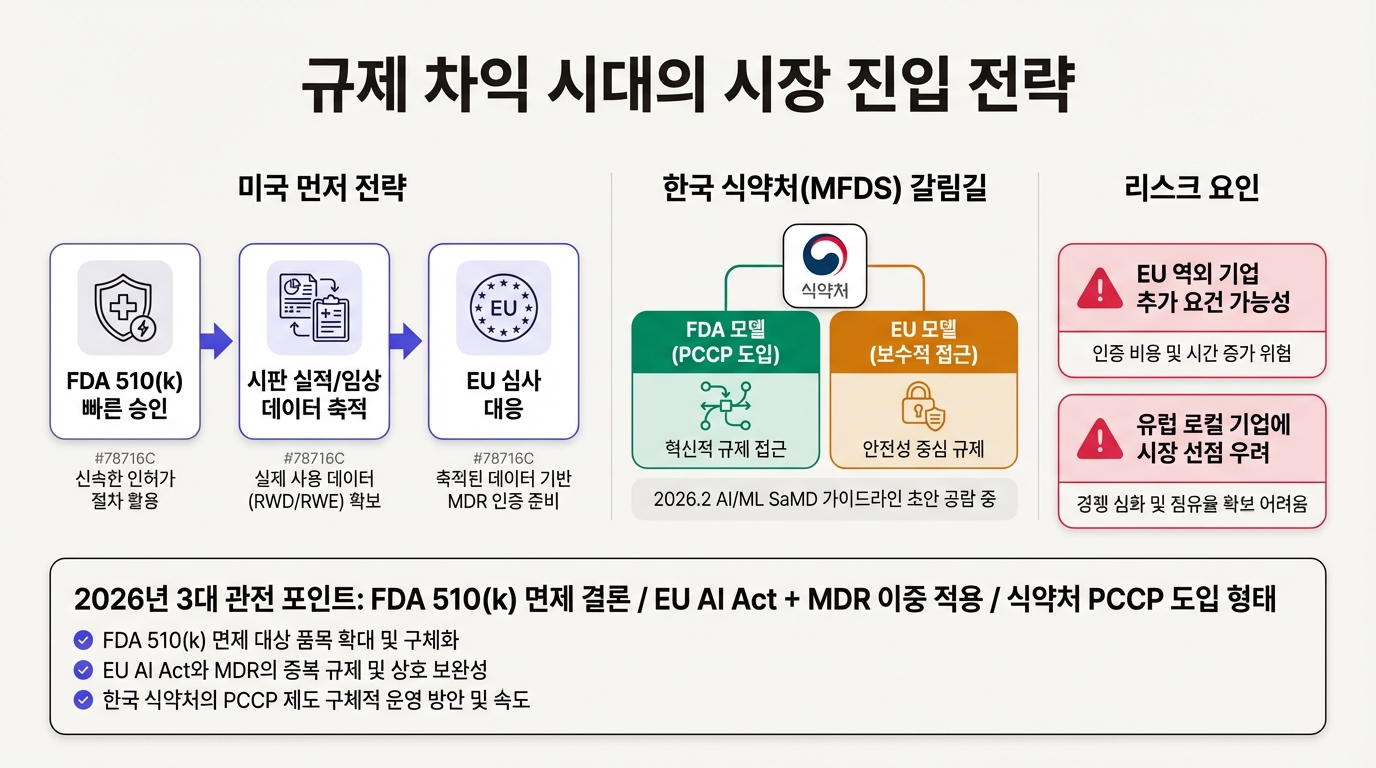
규제 격차가 벌어질수록 AI 의료기기 기업의 시장 진입 전략은 '미국 먼저'로 수렴한다. FDA의 510(k) 경로는 이미 EU MDR보다 예측 가능하고 빠르다. 510(k) 면제까지 현실이 되면 격차는 더 커진다.
숫자가 보여준다. 2025년 한 해 FDA가 승인한 AI/ML 의료기기는 295건. 같은 기간 EUDAMED을 통해 확인 가능한 EU 신규 AI 의료기기 승인은 사실상 추적 불가다. 데이터베이스 자체가 불완전하기 때문이다.
식약처가 서 있는 갈림길
한국 식약처(MFDS)가 흥미로운 위치에 있다. 2026년 2월 16일부터 AI/ML SaMD 품질관리 가이드라인 초안 공람을 시작했고(3월 10일 마감), PCCP 도입 논의가 포함되어 있다. FDA 모델을 따를지, EU의 보수적 접근을 택할지가 핵심이다.
식약처는 이미 생성형 AI 의료기기 허가 심사 가이드라인을 세계 최초로 내놓는 등 선제적으로 움직여왔다. RWE 인정 범위 확대와 AI 심사 시스템 도입도 규제 효율화 방향이다. 2026년 2월 14일에는 루닛 INSIGHT MMG가 클래스 III 허가를 받았다.
식약처가 PCCP를 도입하면 한국 기업에게 흥미로운 경로가 열린다. 국내에서 먼저 PCCP 경험을 쌓고, 이를 발판 삼아 FDA 진출 때 PCCP 승인을 함께 노리는 전략이다. 국내 규제가 글로벌 시장 진출의 테스트베드가 되는 셈이다.
규제 차익이라는 양날의 칼
미국과 EU의 격차는 일종의 규제 차익을 만든다. 같은 제품이라도 시장에 따라 출시 시점이 1~2년 달라질 수 있다. 미국에서 먼저 시판 실적과 임상 데이터를 쌓고, 그 데이터로 EU 심사에 대응하는 순차적 접근이 현실적인 선택이 된다.
다만 리스크가 있다. EU가 AI Act를 본격 시행하면서 역외 기업에 추가 요건을 붙일 수 있고, 미국에만 집중하다 EU 진출 시점을 놓치면 유럽 로컬 기업에게 시장을 내줄 수 있다.
2026년은 AI 의료기기 규제의 분기점이다. FDA가 510(k) 면제 청원에 어떤 결론을 내리는지, EU의 AI Act와 MDR 이중 적용이 실제로 어떤 마찰을 만드는지, 식약처가 PCCP를 어떤 형태로 도입하는지. 이 세 가지가 향후 AI 의료기기 산업의 지형을 결정한다.