2월 한 달 사이, FDA·EU·식약처가 거의 동시에 AI 규제 카드를 꺼냈다. FDA는 2월 2일 QMSR(품질관리시스템 규정)을 발효했고, EU는 2월 16일 MDCG 2026-2를 내놓았으며, 식약처는 2월 14일과 16일 이틀 간격으로 가이드라인 2건을 공개했다. 미국에서만 2월 한 달에 510(k) 승인이 6건 넘게 쏟아지는 상황이니, 규제기관 쪽에서도 기존 프레임워크를 고수할 수 없었을 것이다.
핵심 쟁점은 하나다. 시판 후에도 스스로 학습하고 변하는 AI를 "한 번 허가하면 끝"이라는 전통적 규제 틀에 어떻게 넣을 것인가. 식약처가 내놓은 두 가이드라인은 이 질문에 대한 한국식 답안이다.
PCCP: 알고리즘 업데이트를 미리 약속받는 구조
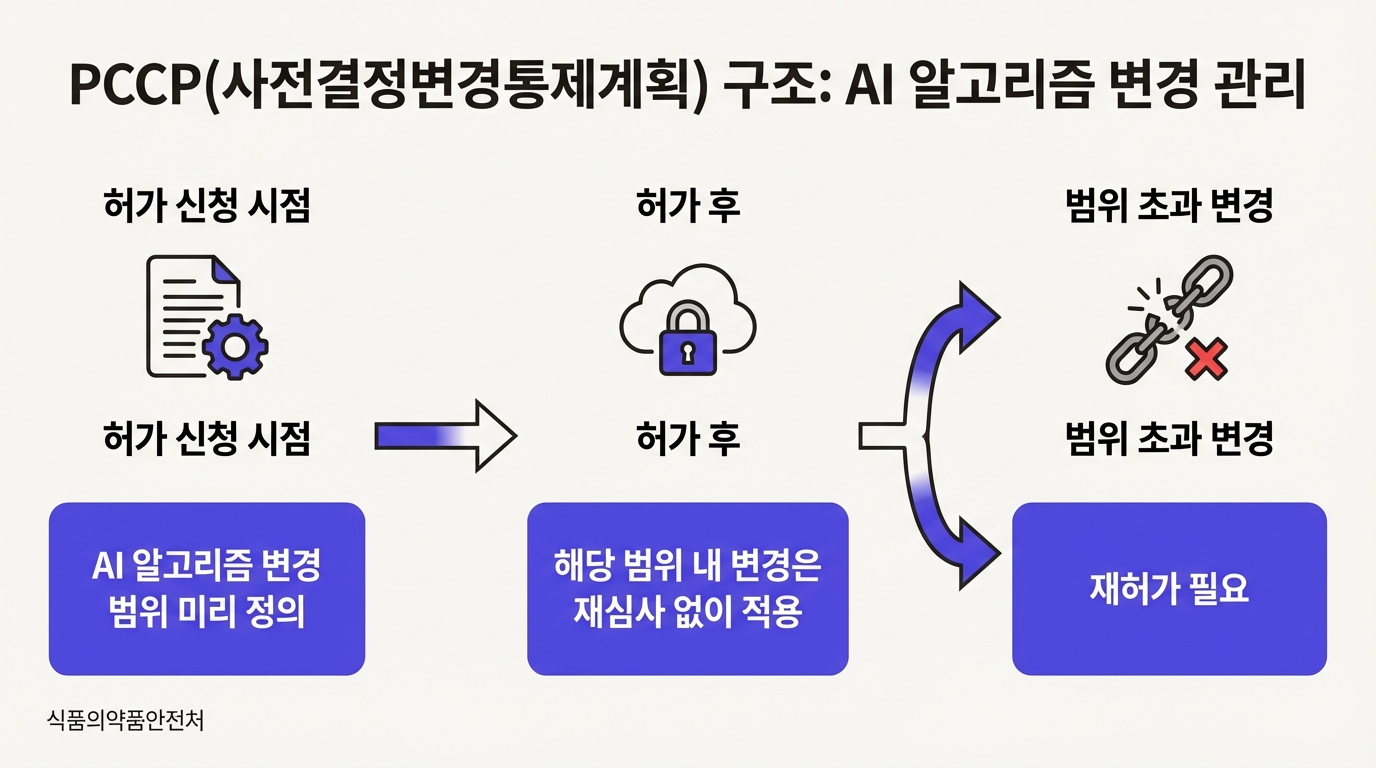
PCCP(Predetermined Change Control Plan)를 풀면 "사전결정변경통제계획"이라는 무시무시한 이름이 되지만, 구조는 직관적이다. AI 의료기기 제조사가 허가를 신청할 때 "향후 이런 조건에서, 이런 데이터로, 이 범위까지 알고리즘을 업데이트하겠다"는 계획서를 함께 낸다. 규제기관이 그 계획 자체를 승인하면, 약속한 범위 안의 변경은 매번 새로 허가를 받지 않아도 된다. 소프트웨어 업데이트마다 허가를 반복하는 비효율을 줄이는 장치인 셈이다.
FDA가 먼저 길을 닦았다. 2023년 파일럿을 시작해, PathAI Prostate(전립선 병리 AI)가 PCCP를 포함한 510(k) 승인을 받은 사례가 나왔다. 재훈련 조건, 사용 데이터, 변경 허용 범위를 구체적으로 명시하고 FDA가 이를 수용한 것이다.
식약처는 2월 16일 품질관리 가이드라인 초안을 공개하면서 PCCP를 한국에 도입하겠다고 선언했다. 의견수렴 마감은 3월 10일. 아직 초안이라 최종 형태는 달라질 수 있지만, PCCP라는 프레임워크 자체를 공식 논의 테이블에 올렸다는 게 포인트다.
한국형 PCCP가 FDA 버전과 어떻게 다를지는 불분명하다. 다만 식약처의 기존 행보에서 단서를 찾을 수 있다. 식약처는 세계 최초로 생성형 AI 의료기기 허가·심사 가이드라인을 발간했다. "생성형 AI"라는 카테고리를 규제 문서에 명시한 것이 FDA나 EU보다 빨랐다는 얘기다. 단순히 FDA를 추종하는 입장이 아니라, 특정 영역에서 앞서가는 전략을 쓰고 있다.
PCCP가 실무에서 중요한 이유는 분명하다. 지금 한국에서 AI 의료기기 알고리즘을 업데이트하려면 변경허가를 다시 받아야 한다. 경미한 수정도 수개월이 걸리는데, 그 사이 글로벌 시장에서는 업데이트된 버전이 돌아간다. PCCP가 자리를 잡으면 사전 합의한 범위 내 업데이트를 별도 허가 없이 진행할 수 있다. 보건복지부가 "혁신적 의료기기 최단 80일 시장 진입"을 밀고 있는 흐름과도 맞물린다.
실시간학습 알고리즘: 허가 이후에도 변하는 AI를 어떻게 감시하나
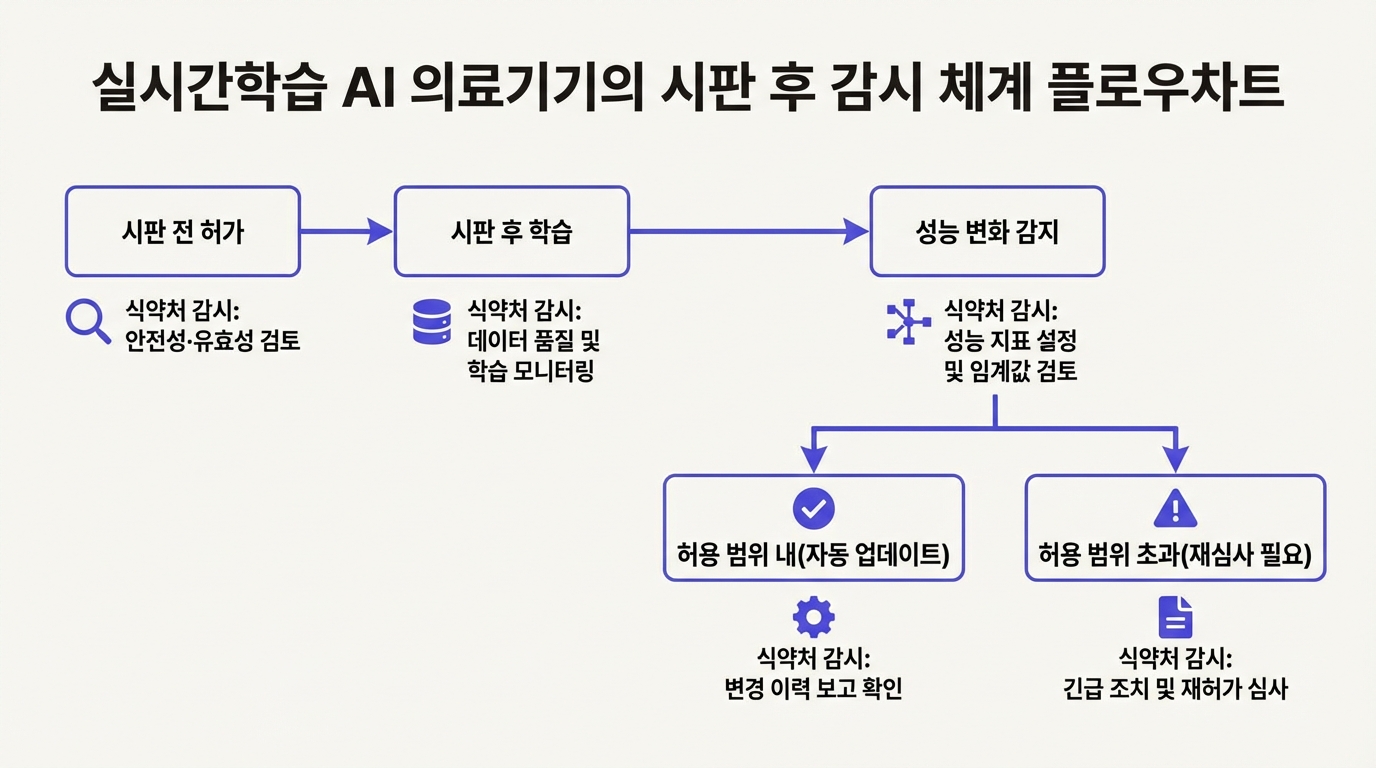
PCCP보다 한 단계 더 까다로운 문제가 있다. 실시간학습(continuous learning) 알고리즘, 즉 시판 후에도 새 데이터를 받아 모델을 스스로 갱신하는 AI다. 보통 AI 의료기기는 훈련을 끝낸 고정 모델(locked algorithm)로 출시된다. 실시간학습 AI는 사용 과정에서 계속 바뀐다.
규제기관이 긴장할 수밖에 없는 구조다. 허가할 때 검증한 성능과 1년 뒤 성능이 다를 수 있다. 성능이 올라갈 수도 있지만, 특정 환자군에서 편향이 생기거나 정확도가 떨어질 가능성도 있다. 허가 시점에 존재하지 않던 리스크가 시판 후에 나타나는 것이다.
식약처는 2월 14일 이 문제에 대한 가이드라인 초안을 공개했다. 의견수렴 마감은 3월 1일로, PCCP보다 2주 가까이 빠르다. 그만큼 긴급도가 높다는 의미다.
글로벌 동향을 보면 FDA는 Medtronic GI Genius의 PMA 보완 승인(2월 16일)에서 실시간 학습 기능 추가를 허용했다. 대장내시경 폴립 검출 AI에 "사용하면서 학습하는" 기능을 더한 것으로, 사례별 허용이 시작된 셈이다. EU도 MDCG 2026-2에서 Continuous Learning 규제 프레임워크를 명시하고 Notified Body의 즉시 적용을 요구했다.
식약처가 FDA·EU와 갈라지는 지점은 무게중심이다. FDA는 PCCP를 통해 "허가 단계에서 변경 범위를 미리 합의"하는 쪽에 초점을 맞춘다. EU는 Notified Body의 지속적 감사로 관리한다. 식약처는 양쪽 요소를 가져오되, 시판 후 안전관리(post-market surveillance)를 별도 가이드라인으로 분리해 규정한다. 더 세분화된 접근이다.
같은 문제, 세 갈래 해법
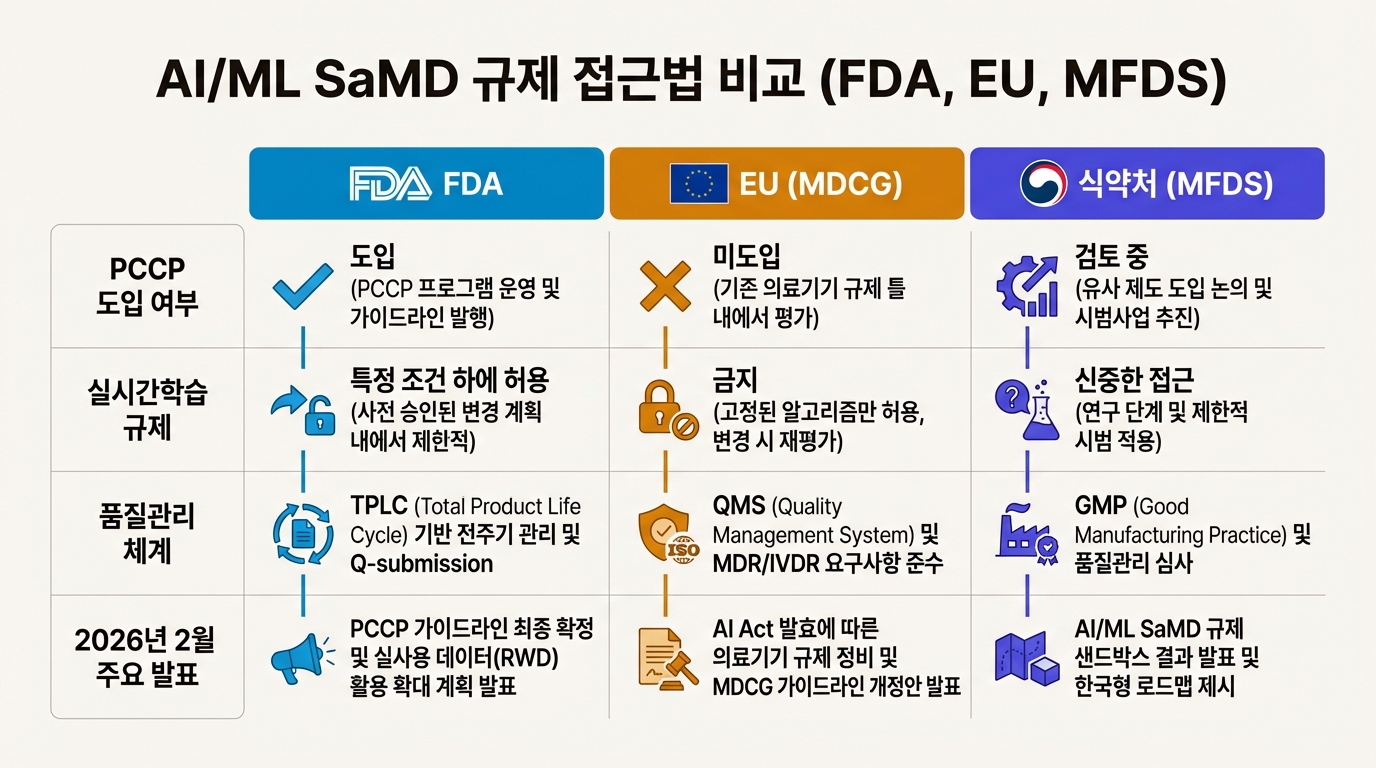
2026년 2월을 기점으로 세 규제기관이 모두 AI 의료기기 규제를 대폭 손보고 있다. 방향은 비슷한데 방법론이 다르다.
FDA는 구조 자체를 정비했다. QMSR 발효로 기존 QSR의 15개 하위 파트를 2개로 줄이고 ISO 13485:2016과 완전히 맞췄다. AI 특화 규제라기보다 의료기기 품질관리 시스템 전반을 현대화한 뒤, 그 위에 PCCP, CDS 규제 완화, 510(k) 면제 청원 등을 얹는 방식이다. 3월에는 AI/ML SaMD 워크숍을 열어 GMLP(Good Machine Learning Practice) 업데이트를 논의할 계획이다.
EU는 MDCG 2026-2로 소프트웨어 변경 관리를 강화했다. Annex IX/XI의 PCCP 요구사항을 높이고, EUDAMED 등록 의무화, 고위험 SaMD 성능 평가 강화를 동시에 추진한다. EU AI Act와 MDR이 동시에 적용되면서 AI/ML SaMD는 Annex XVI 고위험 분류를 받아 Notified Body 검토가 필수가 됐다. 규제가 이중으로 쌓이는 구조다.
식약처는 PCCP와 실시간학습 가이드라인을 별도 문서로 분리해 각각 의견수렴을 진행한다. 여기에 생성형 AI 의료기기 가이드라인(세계 최초), 허가자료 요약·전문 번역·검토서 초안 작성에 AI를 쓰는 심사 시스템까지 도입했다. 규제 대상(AI 의료기기)뿐 아니라 규제 프로세스(심사 자체)에도 AI를 적용하는 양면 전략이다.
기업에게 이것이 의미하는 것
한국 SaMD 기업 입장에서는 득과 실이 동시에 온다.
PCCP가 자리를 잡으면 알고리즘 업데이트 속도가 빨라진다. 혁신적 의료기기 최단 80일 시장 진입이라는 정부 목표와 맞물려 규제 체감 속도가 달라질 수 있다. 2025년에만 혁신의료기기 45개가 지정됐고(전년 29개, 55% 증가), 정부는 5년 내 28개 AI 의료기기 인허가를 목표로 잡았다.
반면 실시간학습 가이드라인은 시판 후 감시 부담을 늘린다. 루닛이 2025년 매출 831억원으로 역대 최대를 기록했지만 EBITDA 흑자 전환은 2026년 말 목표이고, 뷰노는 매출 348억원에 흑자전환 목표가 2026~2027년이다. 아직 흑자를 내지 못하는 상태에서 규제 준수 비용이 추가된다.
FDA·EU·식약처 세 곳의 규제를 모두 충족해야 하는 글로벌 진출 기업에게는 복잡성이 한 겹 더 쌓인다. 각 기관의 PCCP 요구사항, 실시간학습 관리 방식, 품질관리 기준이 미묘하게 다르기 때문이다. "한 번 만들어 세 곳에 제출"하는 전략이 통하지 않을 수 있다. IMed Group과 Firefinch Software가 2월 12일 백서 "Smart Code, Safe Care"에서 UK·US·EU 3개 시장 동시 출시 전략을 다룬 것도 이 복잡성에 대한 업계 고민을 반영한다.
규제는 비용이 아니라 인프라다
식약처의 가이드라인 2건은 단순 규정 추가가 아니다. 생성형 AI 가이드라인에서 보여준 선도적 행보에 이어, AI 의료기기 규제의 두 핵심 난제, 사전 변경 통제와 시판 후 학습 감시를 동시에 꺼냈다.
의료 AI 시장이 2026년 약 7,450억원 규모로 성장할 것이라는 전망, 의료 AI에 1,714억원, AI 복지·돌봄에 2,478억원(전년 대비 2.5배)이라는 예산이 뒷받침하고 있다. 그러나 규제 인프라가 없으면 돈과 기술이 있어도 속도를 낼 수 없다. 식약처의 두 가이드라인은 그 빈 칸을 메우려는 시도다.
3월 1일(실시간학습)과 3월 10일(PCCP), 의견수렴 마감 이후 최종 가이드라인이 어떤 형태로 확정되는지가 올해 한국 AI 의료기기 규제 지형을 결정한다.