병리의 한 명이 하루에 보는 슬라이드
병리의가 전립선 생검 슬라이드 하나를 판독하는 데 5~15분이 걸린다. 12-core 생검이면 슬라이드만 수십 장. 하루에 수십 건의 케이스를 소화해야 하는 병리의에게 전립선 생검은 가장 흔하면서 가장 까다로운 업무다.
까다로운 이유가 있다. Gleason 등급 판정에서 병리의 간 일치율(quadratic weighted kappa)이 0.777~0.916 사이에 분포한다. 같은 조직을 두고 전문가마다 판단이 갈린다. 환자 입장에서 보면 누가 읽느냐에 따라 등급이 달라질 수 있다는 이야기인데, 병리의의 역량 문제가 아니다. 전립선 조직의 Gleason 패턴 자체가 경계가 모호한 연속적 스펙트럼이기 때문이다.
미국에서 전립선암은 남성 암 발생 2위다. 연간 28만 건 이상이 새로 진단되고, 거의 모든 진단에 생검 조직의 Gleason 등급 판정이 수반된다.
그런데 판독을 할 사람이 줄고 있다. 미국 내 활동 중인 병리의는 약 18,000명. AAMC(미국의학교육협의회) 추산으로 현재 인력의 30%가 2030년까지 은퇴한다. 약 5,400명이 빠진다. 병리과 레지던트 매칭 인원은 연간 600명 수준에 정체돼 있고, HRSA(보건자원서비스국)는 2037년까지 병리의 공급이 7% 줄고 수요는 16% 늘 것으로 내다본다. 추가로 3,000명이 필요하다는 계산이다. 인력 충원으로 풀리지 않는 구조적 병목이다.
이 배경에서 2026년 2월 15일, PathAI의 전립선 생검 AI 진단 소프트웨어 PathAI Prostate가 FDA 510(k) 승인(K240592)을 받았다. 95% 이상의 정확도를 입증했고, PCCP(Predetermined Change Control Plan) 승인이 함께 포함됐다. 후자가 더 주목할 대목이다.
PathAI Prostate는 무엇을 하나
PathAI Prostate는 AI/ML 기반 전립선 생검 병리 진단 SaMD(Software as a Medical Device)다. 디지털 스캐너로 촬영한 전립선 생검 조직 슬라이드를 입력받아 암 존재 여부를 검출하고 Gleason 등급을 자동 분류한다.
95% 이상이라는 정확도 수치 자체보다 맥락이 중요하다. PANDA 챌린지(Nature Medicine, 2021)에서 AI 알고리즘이 전문 비뇨기 병리의(uropathologist) 수준의 Gleason 등급 판정 성능을 달성할 수 있음은 이미 확인됐다. 다기관 검증에서 AI의 kappa 값이 0.862~0.868을 기록했는데, 앞서 언급한 병리의 간 일치율 범위(0.777~0.916) 한가운데에 위치한다. AI가 병리의를 대체한다기보다, 병리의 간 편차를 줄여주는 기준점 역할을 한다고 보는 게 정확하다.
임상적 가치는 두 방향에서 나온다. 하나는 미세 암 병소(small foci)를 놓칠 확률을 줄이는 것이다. 전립선 생검에서 위음성(false negative)은 치료 시점을 직접 늦추는 원인이 된다. Paige Prostate 선행 사례에서 AI 보조 판독이 위음성을 70% 줄인 바 있다. 다른 하나는 판독 속도다. 병리의 한 명이 처리할 수 있는 케이스 수가 늘어난다. 인력이 줄어드는 상황에서 효율 개선이 아니라 서비스 유지의 문제다.
PathAI는 이미 AISight Dx라는 디지털 병리 이미지 관리 플랫폼으로 FDA 510(k) 승인을 받았다(2025년 6월). 이번 PathAI Prostate는 그 위에 올라가는 진단 알고리즘이다. 플랫폼과 진단 AI를 한 기업이 동시에 보유하면, 병원 입장에서 슬라이드 관리부터 AI 진단까지 단일 워크플로로 묶을 수 있다.
PCCP가 바꾸는 것들
PCCP(Predetermined Change Control Plan)는 의료기기 제조사가 FDA 승인 시점에 "앞으로 이런 변경을 이렇게 검증하겠다"는 계획을 함께 제출해 사전 승인받는 제도다. 이 계획에 포함된 변경은 이후 별도의 510(k)나 PMA 보충 제출 없이 구현할 수 있다.
AI 의료기기는 데이터가 쌓이면 더 나아진다. 그런데 기존 규제 체계에서는 알고리즘을 업데이트할 때마다 새 심사를 거쳐야 했다. 모델이 좋아졌는데 승인을 다시 받아야 하니 업데이트 주기가 수개월에서 수년으로 늘어졌다. AI의 본질적 장점과 의료기기 규제가 부딪히는 지점이었다.
PCCP는 이 문제를 제도 안에서 풀어낸다. FDA가 2024년 12월 최종 가이던스를 발표했고, 2025년에는 캐나다(Health Canada)와 영국(MHRA)이 PCCP 5대 원칙을 공동 발표했다. 변경 범위를 명확히 정의하고 검증 가능한 것으로 제한(Focused), 환자 안전 중심의 위험 평가를 수반(Risk-based), 적절한 데이터와 검증으로 뒷받침(Evidence-based), 규제 기관과 이해관계자에게 투명하게 소통(Transparent)이 골자다.
PathAI는 이미 선례를 만들어뒀다. 2025년 6월 AISight Dx의 1차 진단(primary diagnosis) 510(k) 승인에 PCCP가 포함됐고, 2025년 8월에는 이 PCCP를 활용해 별도 510(k) 없이 Roche VENTANA DP 200/DP 600 스캐너 호환을 추가했다. AISight Dx는 디지털 병리 이미지 관리 소프트웨어 중 최초로 PCCP 승인을 받은 제품이며, 2025년 7월 기준 전체 510(k) 데이터베이스에서 PCCP 승인을 받은 기기는 60개가 채 되지 않았다.
이번 PathAI Prostate의 PCCP가 한 단계 더 나간 이유가 있다. 이미지 관리가 아니라 진단 알고리즘 자체에 적용됐기 때문이다. 새 훈련 데이터로 Gleason 등급 판정 정확도를 올리거나 새 암 유형 분류를 추가하는 작업이 별도 심사 없이 가능해졌다(PCCP 명시 범위 내에서).
비즈니스 모델에 미치는 영향도 있다. 정기적 성능 업데이트가 규제 장벽 없이 이루어지면, 구독 모델의 논리가 규제적으로 뒷받침된다. 계속 좋아지는 제품에 지속적으로 비용을 지불하는 SaaS형 의료기기가 성립하는 것이다.
Paige, Ibex, Aiforia: 누가 뭘 갖고 있나
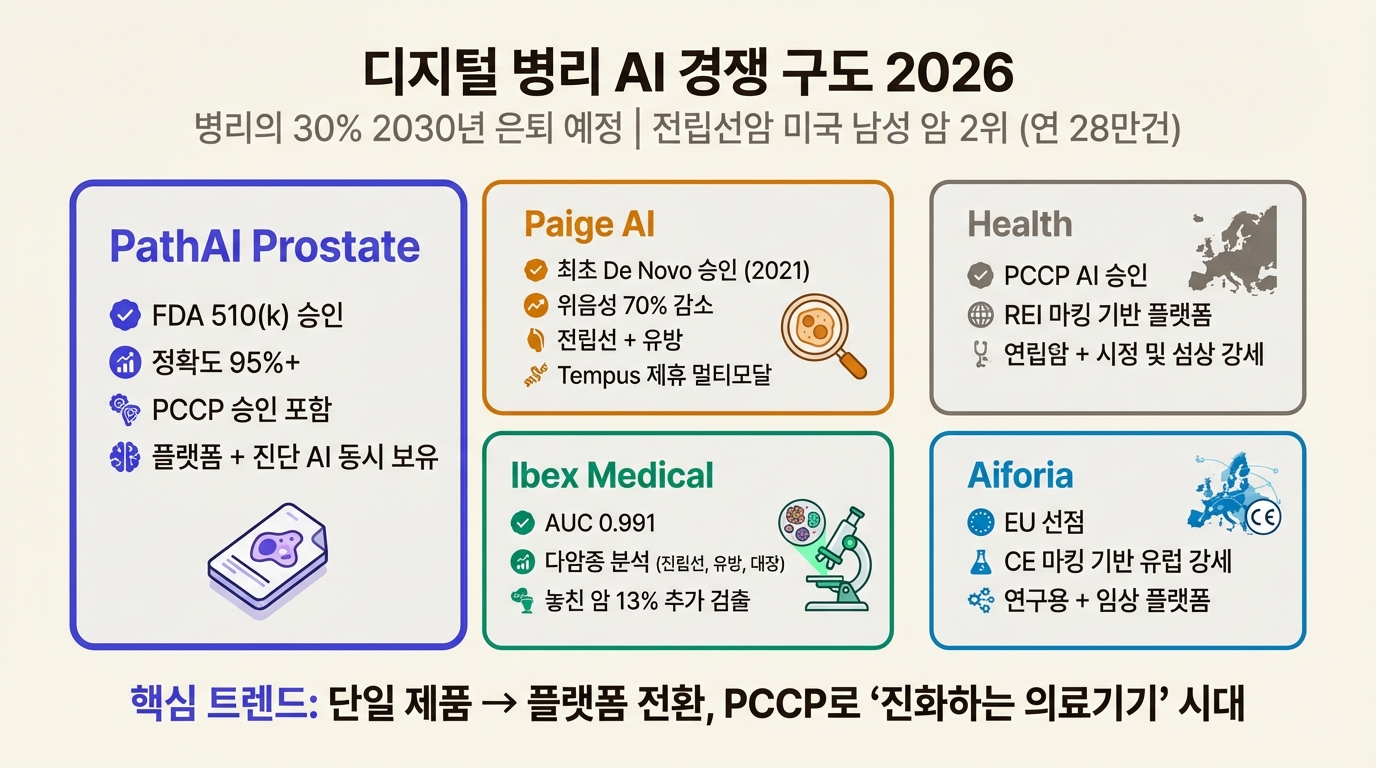
PathAI Prostate가 진입한 시장에는 이미 자리잡은 기업이 있다.
Paige AI는 2021년 디지털 병리 AI 최초의 FDA De Novo 승인을 받았다. Paige Prostate가 첫 제품으로, 전립선 생검에서 암 의심 영역을 자동 검출한다. 임상 연구에서 위음성을 70%, 위양성을 24% 줄였다. 2025년에는 Tempus와 제휴해 병리+게놈 데이터를 결합한 멀티모달 플랫폼으로 확장 중이다.
Ibex Medical Analytics는 이스라엘 기반으로, Galen 플랫폼을 통해 전립선암·유방암·대장암 등 여러 암종을 동시에 커버한다. FDA 510(k) 승인을 받은 Ibex Prostate Detect는 AUC 0.991의 암 검출 성능에 신경주위 침윤(perineural invasion) 자동 검출(AUC 0.957)까지 지원한다. 병리의가 초기 판독에서 놓친 전립선암의 13%를 추가로 잡아냈다는 데이터가 눈에 띈다.
Aiforia는 핀란드 기반으로 유럽 시장에 강하다. CE 마킹을 활용한 유럽 진입이 빠르고, 유방암 진단 AI로 EU 인증을 확보했다. 연구용 AI 분석 플랫폼과 임상 진단 제품을 함께 운영하면서 유럽 규제 인증 자체를 경쟁 방어막으로 쓰고 있다.
Paige가 "최초"라는 타이틀을 쥐고 있다면, Ibex는 다암종 커버리지, Aiforia는 유럽 선점이 강점이다. PathAI가 내세울 카드는 PCCP다.
시장 전체 흐름은 단일 질환 솔루션에서 멀티모달 플랫폼으로 이동하고 있다. 슬라이드 수준의 픽셀 검출과 효율 개선에서, 환자 수준의 예후 예측과 치료 반응 분석으로 넘어가는 과정이다. Tempus-Paige 제휴, PathAI의 플랫폼+진단 AI 이중 전략이 이 흐름을 보여준다. AI 기반 디지털 병리 시장은 2025~2035년 사이 빠른 성장이 예상되며, AI 병리 품질관리 시장만으로도 2029년 38.4억 달러 규모가 전망된다.
플랫폼과 PCCP를 동시에 쥔 기업
개별 요소만 놓고 보면 PathAI가 압도적이라고 말하기 어렵다. 그런데 두 가지를 동시에 가졌다는 데서 차이가 생긴다.
AISight Dx(이미지 관리 플랫폼)와 PathAI Prostate(진단 알고리즘)를 모두 보유한다. 병원이 하나의 벤더로 슬라이드 스캐닝부터 이미지 관리, AI 진단까지 묶을 수 있으면 도입 장벽이 낮아진다.
여기에 플랫폼과 진단 AI 양쪽 모두에 PCCP를 확보했다. AISight Dx는 스캐너·디스플레이·브라우저 호환 확장에, PathAI Prostate는 알고리즘 업데이트에 PCCP를 쓴다. 경쟁사가 새 스캐너 호환이나 알고리즘 업데이트마다 510(k)를 다시 제출하는 동안, PathAI는 PCCP 범위 내에서 바로 시장에 반영할 수 있다. 하드웨어 호환성과 소프트웨어 성능 양쪽에서 움직임이 빠른 셈이다.
이 격차는 시간이 갈수록 벌어진다. PCCP가 아직 60개 미만의 기기에만 적용된 초기 단계라는 점을 감안하면, 규제 전략 자체가 진입 장벽이 되고 있다.
식약처 PCCP 가이드라인이 나왔다
한국 식약처(MFDS)는 2026년 2월 16일 AI/ML SaMD 품질관리 가이드라인 초안 공람을 시작했다(의견 마감 3월 10일). 이 가이드라인에 PCCP 도입 논의가 포함돼 있다.
같은 시기에 대서양 건너 EU는 반대로 움직이고 있다. EU의 MDCG 2026-2 가이드라인(2026년 2월 16일)은 AI/ML SaMD의 소프트웨어 변경 관리에 대해 PCCP 요구를 오히려 강화했다. 같은 제도를 두고 미국은 유연하게, EU는 엄격하게 접근한다. 식약처가 어느 쪽에 가까운 입장을 취하느냐가 국내 AI 의료기기 기업의 글로벌 전략에 직접 연결된다.
국내 현황을 보면 루닛 컨소시엄이 과기부 '인공지능 특화 파운데이션 모델 프로젝트' 의과학 분야 주관기관으로 선정돼 2026년 9월까지 개발을 진행 중이다. 루닛의 SCOPE 제품군은 바이오마커 분석 기반 SaMD로, 디지털 병리 영역에서 한국 기업의 기술력을 보여준다. 다만 전립선 생검 Gleason 등급 판정이라는 특정 영역에서 PathAI, Paige, Ibex와 직접 경쟁하는 국내 제품은 아직 없다.
정부의 의료 AI 투자(1,714억원), 혁신의료기기 지정 확대(2025년 45개, 전년 대비 1.5배), AI/ML SaMD 가이드라인 정비는 인프라 측면에서 긍정적이다. 다만 두 가지 병목이 남아 있다. 수가 체계(1군 2,920원)가 AI 도입의 경제적 유인을 제한하고, 디지털 병리의 전제 조건인 전체 슬라이드 스캐너(WSI) 도입률 자체가 선진국 대비 낮다. 스캐너가 없으면 디지털 병리 AI를 쓸 수 없다. 인프라가 먼저다.
PathAI Prostate의 PCCP 승인이 보여주는 방향은 분명하다. AI 의료기기 규제의 무게중심이 "최초 승인"에서 "승인 후 업데이트 관리"로 옮겨가고 있다. 식약처가 이 흐름을 얼마나 빠르게 받아들이느냐가 국내 AI 의료기기 기업의 글로벌 경쟁력을 가를 변수다.